基因工程基因工程到底是什么?
什么是基因工程?它包括哪些主要步骤
基因工程(ic engineering)又称基因拼接技术和DNA重组技术,是以分子遗传学为理论基础,以分子生物学和微生物学的现代方法为手段,将不同来源的基因按预先设计的蓝图,在体外构建杂种DNA分子,然后导入活细胞,以改变生物原有的遗传特性、获得新品种、生产新产品。第一步,获取目的基因。
第二步,目的基因与运载体结合。
第三步,将目的基因导入受体细胞。
第四步,目的基因的检测与鉴定。
什么是基因工程?
是基因工程吧 基因工程简介 我们常常说基因是生物体进行生命活动的“蓝图”,这是因为生物体可以通过基因的特异性表达,来完成各种生命活动。例如,青霉菌能够产生出对人类有用的抗生素——青霉素;豆科植物的根瘤菌能够固定空气中的氮;家蚕能够吐出丝……那么,人们能不能通过改造生物体的基因,定向地改变生物的遗传特性呢?比如,通过对基因进行改造和重新组合,让禾本科的植物也能够固定空气中的氮,让细菌“吐出”蚕丝,让微生物生产出人的胰岛素、干扰素等珍贵的药物。
科学家们经过多年的努力,终于在20世纪70年代,创立了一种能够定向改造生物的新技术——基因工程。
那么,什么是基因工程呢?基因工程又是怎样改变生物遗传特性的呢? 一 基因工程的基本内容 基因工程又叫做基因拼接技术或DNA重组技术。
这种技术是在生物体外,通过对DNA分子进行人工“剪切”和“拼接”,对生物的基因进行改造和重新组合,然后导入受体细胞内进行无性繁殖,使重组基因在受体细胞内表达,产生出人类所需要的基因产物。
通俗地说,就是按照人们的主观意愿,把一种生物的个别基因复制出来,加以修饰改造,然后放到另一种生物的细胞里,定向地改造生物的遗传性状。
基因工程是在DNA分子水平上进行设计施工的。
DNA分子的直径只有2.0nm(粗细只有头发丝的十万分之一),其长度也是极其短小的。
如流感嗜血杆菌的DNA,长度只有0.83?m,即使是较大的大肠杆菌,其长度也只有1.36?m。
要在如此微小的DNA分子上进行剪切和拼接,是一项非常精细的工作,必须要有专门的工具。
基因操作的工具 用什么样的工具才能准确无误地对基因进行剪切和拼接呢?这是从事基因工程研究的科学家首先遇到的难题。
例如,通过基因工程培育抗虫棉时,就需要将抗虫的基因从某种生物(如苏云金芽孢杆菌)中提取出来,“放入”棉的细胞中,与棉细胞中的DNA结合起来,在棉中发挥作用。
这里遇到的难题主要有两个:首先是苏云金芽孢杆菌的一个DNA分子有许多基因,怎样从它的DNA分子的长链上辨别出所需要的基因,并且把它切割下来。
其次是如何将切割下来的抗虫基因与棉的DNA“缝合”起来。
为了突破这些难关,科学家进行了许多试验,最后他们发现了一种“基因剪刀”和“基因针线”,可以用来完成基因的剪切和拼接。
基因的剪刀——限制性内切酶 基因的剪刀指的是DNA限制性内切酶(以下简称限制酶)。
限制酶主要存在于微生物中。
一种限制酶只能识别一种特定的核苷酸序列,并且能在特定的切点上切割DNA分子(如图)。
例如,从大肠杆菌中发现的一种限制酶只能识别GAATTC序列,并在G和A之间将这段序列切开。
目前已经发现了二百多种限制酶,它们的切点各不相同。
苏云金芽孢杆菌中的抗虫基因,就能被某种限制酶切割下来。
基因的针线——DNA连接酶 从图中可以看出,被限制酶切开的DNA两条单链的切口,带有几个伸出的核苷酸,它们之间正好互补配对,这样的切口叫做黏性末端。
可以设想,如果把两种来源不同的DNA用同一种限制酶来切割,然后让两者的黏性末端黏合起来,似乎就可以合成重组的DNA分子了。
但是,实际上仅仅这样做是不够的,互补的碱基处虽然连接起来,但是这种连接只相当于把断成两截的梯子中间的踏板连接起来,两边的扶手的断口处还没有连接起来(如图)。
要把扶手的断口处连接起来,也就是把两条DNA末端之间的缝隙“缝合”起来,还要靠另一种极其重要的工具——DNA连接酶。
基因的运输工具——运载体 要将一个外源基因,如上面所说的抗虫基因,送入受体细胞,如棉细胞,还需要有运输工具,这就是运载体。
作为运载体的物质必须具备以下条件:能够在宿主细胞中复制并稳定地保存;具有多个限制酶切点,以便与外源基因连接;具有某些标记基因,便于进行筛选。
目前,符合上述条件并经常使用的运载体有质粒、噬菌体和动植物病毒等。
质粒是基因工程最常用的运载体,它广泛地存在于细菌中,是细菌染色体外能够自主复制的很小的环状DNA分子,大小只有普通细菌染色体DNA的百分之一(如图)。
质粒能够“友好”地“借居”在宿主细胞中。
一般来说,质粒的存在与否对宿主细胞生存没有决定性的作用。
但是,质粒的复制则只能在宿主细胞内完成。
大肠杆菌、枯草杆菌、土壤农杆菌等细菌中都有质粒。
因为土壤农杆菌很容易感染植物细胞,所以科学家培育转基因植物时,常常用土壤农杆菌中的质粒做运载体。
基因操作的基本步骤 进行基因操作一般要经历四个基本步骤,也就是基因操作的“四步曲”。
提取目的基因 基因操作的第一步,是取得人们所需要的特定基因,也就是目的基因(如图)。
如前 面提到的苏云金芽孢杆菌中的抗虫基因,还有植物的抗病(抗病毒、抗细菌)基因、 种子的贮藏蛋白的基因,以及人的胰岛素基因、干扰素基因等,都是目的基因。
要从浩瀚的“基因海洋”中获得特定的目的基因,犹如大海捞针,是十分不易的。
科学家们经过不懈地探索,想出了许多办法,概括地说,主要有两条途径:一条是从供体细胞的DNA中直接分离基因;另一条是人工合成基因。
直接分离基因最常用的方法是“鸟枪法”,又叫“散弹射击法”。
这种方法犹如用猎枪发射的散弹打鸟,无论哪一颗弹粒击中目标,都能把鸟打下来。
鸟枪法的具体做法是:用限制酶将供体细胞中的DNA切成许多片段,将这些片段分别载入运载体,然后通过运载体分别转入不同的受体细胞,让供体细胞所提供的DNA(外源DNA)的所有片段分别在各个受体细胞中大量复制(在遗传学中叫做扩增),从中找出含有目的基因的细胞,再用一定的方法把带有目的基因的DNA片段分离出来。
如许多抗虫、抗病毒的基因都可以用上述方法获得。
用“鸟枪法”获取目的基因的缺点是工作量大,具有一定的盲目胜。
又由于真核细胞的基因含有不表达的DNA片段,不能直接用于基因的扩增和表达,因此,在获取真核细胞中的目的基因时,一般是用人工合成基因的方法。
目前人工合成基因的方法主要有两条途径。
一条途径是以目的基因转录成的信使RNA为模板,反转录成互补的单链DNA,然后在酶的作用下合成双链DNA,从而获得所需要的基因。
另一条途径是根据已知的蛋白质的氨基酸序列,推测出相应的信使RNA序列,然后按照碱基互补配对原则,推测出它的结构基因的核苷酸序列,再通过化学的方法,以单核苷酸为原料合成目的基因(如图)。
如人的血红蛋白基因、胰岛素基因等就可以通过人工合成基因的方法获得。
20世纪80年代以后,随着DNA核苷酸序列分析技术的发展,人们已经可以通过DNA序列自动测序仪(见本章题图左上照片)对提取出来的基因进行核苷酸序列分析,并且通过一种扩增DNA的新技术(也叫PCR技术),使目的基因片段在短时间内成百万倍地扩增。
上述新技术的出现大大简化了基因工程的操作技术。
目的基因与运载体结合 将目的基因与运载体结合的过程,实际上是不同来源的DNA重新组合的过程。
如果以质粒作为运载体,首先要用一定的限制酶切割质粒,使质粒出现一个切口,露出黏性末端。
然后用同一种限制酶切断目的基因,使其产生相同的黏性末端。
将切下的目的基因的片段插入到质粒的切口处,再加入适量的DNA连接酶,质粒的黏性末端与目的基因DNA片段的黏性末端就会因碱基互补配对而结合,形成了一个重组DNA分子(如图)。
如人的胰岛素基因就是通过这种方式与大肠杆菌中的质粒DNA分子结合,形成重组DNA分子(也叫重组质粒)的。
将目的基因导入受体细胞 目的基因的片段与运载体在生物体外连接形成重组DNA分子后,下一步是将重组DNA分子引入受体细胞中进行扩增(如图)。
基因工程中常用的受体细胞有大肠杆菌、枯草杆菌、土壤农杆菌、酵母菌和动植物细胞等。
用人工的方法使体外重组的DNA分子转移到受体细胞,主要是借鉴细菌或病毒侵染细胞的途径。
例如,如果运载体是质粒,受体细胞是细菌,一般是将细菌用氯化钙处理,以增大细菌细胞壁的通透性,使含有目的基因的重组质粒进入受体细胞。
目的基因导入受体细胞后,就可以随着受体细胞的繁殖而复制,由于细菌繁殖的速度非常快,在很短的时间内就能够获得大量的目的基因。
目的基因的检测和表达 以上步骤完成以后,在全部受体细胞中,真正能够摄入重组DNA 分子的受体细胞是很少的。
因此,必须通过一定的手段对受体细胞中是否导入了目的基因进行检测。
检测的方法有很多种,例如,大肠杆菌的某种质粒具有青霉素抗性基因,当这种质粒与外源DNA组合在一起形成重组质粒,并被转入受体细胞后,就可以根据受体细胞是否具有青霉素抗性来判断受体细胞是否获得了目的基因。
重组的DNA分子进入受体细胞后,受体细胞必须表现出特定的性状,才能说明目的基因完成了表达过程。
例如,科学家最初做抗虫棉试验时,虽然已经检测出棉的植株中含有抗虫的基因,但让棉铃虫食用棉的叶片时,棉铃虫并没有被杀死,这说明抗虫基因还不能在高等植物中表达。
科学家在研究的基础上,又一次对棉植株中的抗虫基因进行了修饰,然后再让棉铃虫食用棉的叶片,结果食用的第二天棉铃虫就中毒死亡了。
这说明抗虫基因在棉植株中得到了表达
什么是基因工程?
基因工程也称为遗传工程、基因拼接技术或DNA重组技术。
这种技术是在生物体外,通过对DNA分子进行人工“剪接”和“拼接”,对生物的基因进行改造和重新组合,然后导入受体细胞内进行无性繁殖,使重组基因在受体细胞内表达,产生出人类所需要的基因产物。
基因工程是生物技术的主体技术。
基因工程是指按照人类的愿望,将不同生物的遗传物质在体外人工剪切并和载体重组后转入细胞内进行扩增,并表达产生所需蛋白质的技术。
基因工程能够打破种属的界限,在基因水平上改变生物遗传性,并通过工程化为人类提供有用产品及服务。
基因工程到底是什么?
【摘要与前言】 基因工程技术,在医药及农业上应用广泛。这项尖端科技加上最近突破性的生殖科技,却引发人们极大的隐忧及争论。
生物学家在一百多年前就知道,生物的表征遗传自其亲代。
生物细胞的细胞核,含有染色体,组成分为DNA。
DNA含有四种碱基(简称A、T、C、G)。
这些碱基在DNA中看似杂乱无章,但它们的排列顺序,正代表遗传讯息。
每三个碱基代表一种胺基酸的密码。
基因就是这些遗传密码的组合,亦即代表蛋白质的胺基酸序列。
每个基因含有启动控制区,以调控基因的表达。
基因工程是一项很精密的尖端生物技术。
可以把某一生物的基因转殖送入另一种细胞中,甚至可把细菌、动植物的基因互换。
当某一基因进入另一种细胞,就会改变这个细胞的某种功能。
基因工程对于人类的利弊一直是个争议的问题,主要是这项技术创造出原本自然界不存在的重组基因。
但它为医药界带来新希望,在农业上提高产量改良作物,也可对环境污染、能源危机提供解决之道,甚至可用在犯罪案件的侦查。
但它亦引起很大的忧虑与关切。
当此科技由严谨的实验室转移至大规模医药应用或商业生产时,我们如何评估它的安全性?此项技术是否可能因为人为失控,反而危害人类健康并破坏大自然生态平衡? 【正文】 观点:辨证的看待基因工程的利与弊 一.基因工程可用来筛检及治疗遗传疾病。
遗传疾病乃是由于父或母带有错误的基因。
基因筛检法可以快速诊断基因密码的错误;基因治疗法则是用基因工程技术来治疗这类疾病。
产前基因筛检可以诊断胎儿是否带有遗传 疾病,这种筛检法甚至可以诊断试管内受精的胚胎,早至只有两天大,尚在八个细胞阶段的 试管胚胎。
做法是将其中之一个细胞取出,抽取DNA,侦测其基因是否正常,再决定是否把此胚胎植入母亲的子宫发育。
胎儿性别同时也可测知。
但是广泛的基因筛检将会引起一连串的社会问题。
如果有人接受基因筛检,发现在某个年龄将因某种病死亡,势必将会极度改变他的人生观。
虽然基因筛检可帮助医生更早期更有效地治疗病人,但可能妨碍他的未来生活就业。
譬如人寿保险公司将会要求客户提供家族健康数据,如心脏病、糖尿病、乳癌等,而针对高危险群家族成员设定较高的保费。
保险公司可由基因筛检资料预知客户的预估寿命。
这些人可能因而得不到保险的照顾,也可能使这些人被公司老板提早解聘。
二.基因工程配合生殖科技——全人类的震撼 基因筛检并不改变人的遗传组成,但基因治疗则会。
科学家正努力改变遗传病人的错误基因,把好的基因送入其中以纠正错误。
因为这是在操作生命的基本问题,必须格外小心。
首先须划分医疗及非医疗的行为。
医疗行为目的在治病,非医疗者如想提高孩子的身高、智慧等。
选择胎儿性别也是非医疗行为,不能被接受,但是遇到某些性连遗传的疾病,选择胎儿的性别就是可被接受的医疗行为。
另一项须区分的,就是体细胞(somatic cell)或生殖细胞(germ-line cell)的基因操作。
体细胞的基因操作只影响身体的体细胞,不影响后代。
但卵子、精子等生殖细胞之基因操作,会直接影响后代,目前基因工程禁止直接用在生殖细胞上。
三.基因治疗法——遗传病人的福音 目前医学界正在临床试验多种遗传病的基因治疗法。
最早采用基因治疗的是一种先天免疫缺乏症,又称气泡男孩症(bubble-boy disease),患病婴幼童因为腺脱胺(adenosine deaminase)基因有缺陷,骨髓不能制造正常白血球发挥免疫功能,必须生活在与外界完全隔离的空气罩内。
最新的治疗法是由病人骨髓分离出白血球的干细胞,把正常的酵素基因接在经过改造不具毒性的反录病毒(retrovirus),藉此病毒送入白血球干细胞,再将干细胞送回病人体内,则病人可产生健康的白血球获得免疫功能。
这项临床试验,在美国的女病童证明很成功。
另一种较便捷的治疗法亦在实验中,纤维性囊肿(cystic fibrosis)在英国平均每两千人中就有一人罹患此症。
病人无法制造形成细胞膜氯离子通道的蛋白。
此蛋白分布于分泌性细胞的胞膜上,控制氯离子的运输,使黏液畅通。
病人体内因缺乏此蛋白,体内浓黏液堆积阻塞肺部通道,甚至发炎死亡。
为了治疗此病,目前正在发展新方法,将正常基因加入雾状喷剂中,病人可借着吸入喷剂,使基因进入肺细胞产生蛋白,达到治疗目的。
四.农林渔牧的应用——生态环保的顾虑 目前全世界正重视发展永续性农业(sustainable agriculture),希望农业除了具有经济效益,还要生生不息,不破坏生态环境。
基因工程正可帮忙解决这类问题。
基因工程可以改良农粮作物的营养成分或增强抗病抗虫特性。
可以增加畜禽类的生长速率、牛羊的泌乳量、改良肉质及脂肪含量等。
英国爱丁堡科学家已经可以使绵羊分泌含有人类抗胰蛋白(α-1-antitryspin)的羊奶。
抗胰蛋白可以治疗遗传性肺气肿,价格很昂贵。
若以后能由羊奶大量制造,将变得很便宜。
但是目前以基因工程开发培育基因转殖绵羊的过程,仍是很费时费钱的。
基因转殖的细菌用处也很大,如改造细菌可以消化垃圾废纸,而这些细菌又可成为一种 蛋白质的营养来源。
基因转殖的细菌可带有人类基因,以生产医疗用的胰岛素及生长激素等。
其实基因工程在农业上的应用,在某些方面而言并不稀奇。
自古以来,人们即努力而有计划地进行育种,譬如一个新种小麦,乃是经过上千代重复杂交育成的。
目前的小麦含有许 多源自野生黑麦的基因。
农人早在基因工程技术发明以前,就知道将基因由一种生物转移至另一生物。
传统的育种也可大量提高产量。
但是传统的育种过程缓慢,结果常常难以预料。
基因工程可选择特定基因送入生物体内,大大提高育种效率,更可把基因送入分类上相差很远的生物,这是传统的育种做不到的。
不久,在美国即将有基因工程培育出来的西红柿要上市了。
这种西红柿含有反意基因(antisense gene),能使西红柿成熟时不会变软易烂。
基因工程也生产抗病抗虫作物,使作物本身制造出“杀虫剂”。
如此农夫就不需费力喷洒农药,使我们有健康的生活环境。
也可培育出抗旱耐盐作物以适合生长在恶劣的环境下,如此可克服第三世界的粮食短缺问题。
但是,会产生“杀虫剂”的作物,也可能对大环境有害,它们或许会杀死不可预期的益虫,影响昆虫生态的平衡。
在高盐的沼泽地种植基因工程育成的作物,可能会干扰了生态系统。
假如热带作物改造得可以于温带地区生长,可能会严重伤害开发中国家的经济,因为农作物水果的输出是他们的主要收入。
最近更逐渐发现危害作物的害虫,已经慢慢地演化,以抵抗基因转殖作物所产生的「杀虫剂」了。
基因工程培育的鱼,也引起一连串的问题。
目前已送两个基因到鲤鱼中,一是生长激素,一是抗冻蛋白(antifreeze protein)。
若有人不小心或刻意地把这些鱼放入自然环境的河、湖中,将会严重影响自然界的鱼群生态。
五.基因转殖动物——爱护动物人士的关切 基因转殖动物对于生物医学研究,真是一大恩赐。
科学家现在可将基因送入实验室的老鼠,以研究基因的表达调控功能。
也可以把实验动物的某个基因刻意破坏,培育出患有类似人类遗传疾病的动物,以利治疗方法的探讨。
美国一家公司已经培育出一种基因转殖老鼠,它在数个月大时会长出癌瘤,此项发明正在申请专利。
但是爱护动物人士已表示严重关切,他们认为应该限制基因工程技术如此折磨虐待实验动物。
(注:基因工程的应用并不只有以上部分,我只对以上部分发表个人观点。
) 【结语】 不久的将来,基因工程技术仍只限于转殖少数的基因,如此培育出来的生物仍将是我们熟悉的生物。
但是有很多疾病及生物特征是由多数基因决定的,而且基因常常不是独立行使功能,它们会受环境的影响。
譬如一组基因会造成某人罹患气喘,但症状受生活的环境影响很大。
一个人罹患糖尿病的机率,也与环境因子(饮食条件)息息相关。
一个天才钢琴家的音乐天赋包括听力及灵敏的双手巧妙地配合,这跟他的遗传基因、童年音乐的启发、生活环境等都有关连。
所以我们在还未了解基因与环境因子的互动关系前,还不能奢望创造出具有超高智商的人,或是利用基因筛检法筛选出具有特殊天赋的孩子。
21世纪是基因工程技术蓬勃发展的时代,基因工程的兴起是生物革命的必然结果,尽管基因工程的隐忧及争论众说纷纭,但其给人带来的好处是显而易见的。
希望随着生物界的不断发展,使基因工程的安全性得到保证,让人们在生活的各个方面都能感受基因工程给人类带来的利益
- 基因工程基因工程到底是什么?相关文档
- 基因工程什么是基因工程
- 基因工程基因工程的概念
- 基因工程什么是基因工程?
- 基因工程什么是基因工程?
DiyVM(50元起)老牌商家,香港沙田CN2直连vps/不限流量/五折终身优惠
diyvm怎么样?diyvm是一家国内成立时间比较久的主机商家了,大约在6年前站长曾经用过他家的美国机房的套餐,非常稳定,适合做站,目前商家正在针对香港沙田机房的VPS进行促销,给的是五折优惠,续费同价,香港沙田机房走的是CN2直连的线路,到大陆地区的速度非常好,DiyVM商家采用小带宽不限流量的形式,带宽2Mbps起步,做站完全够用,有需要的朋友可以入手。diyvm优惠码:五折优惠码:OFF50...
美国高防云服务器 1核 1G 26元/月 香港/日本站群服务器 E5 16G 1600元/月 触摸云
触摸云国内IDC/ISP资质齐全商家,与香港公司联合运营, 已超8年运营 。本次为大家带来的是双12特惠活动,美国高防|美国大宽带买就可申请配置升档一级[CPU内存宽带流量选一]升档方式:CPU内存宽带流量任选其一,工单申请免费升级一档珠海触摸云科技有限公司官方网站:https://cmzi.com/可新购免费升档配置套餐:地区CPU内存带宽数据盘价格购买地址美国高防 1核 1G10M20G 26...
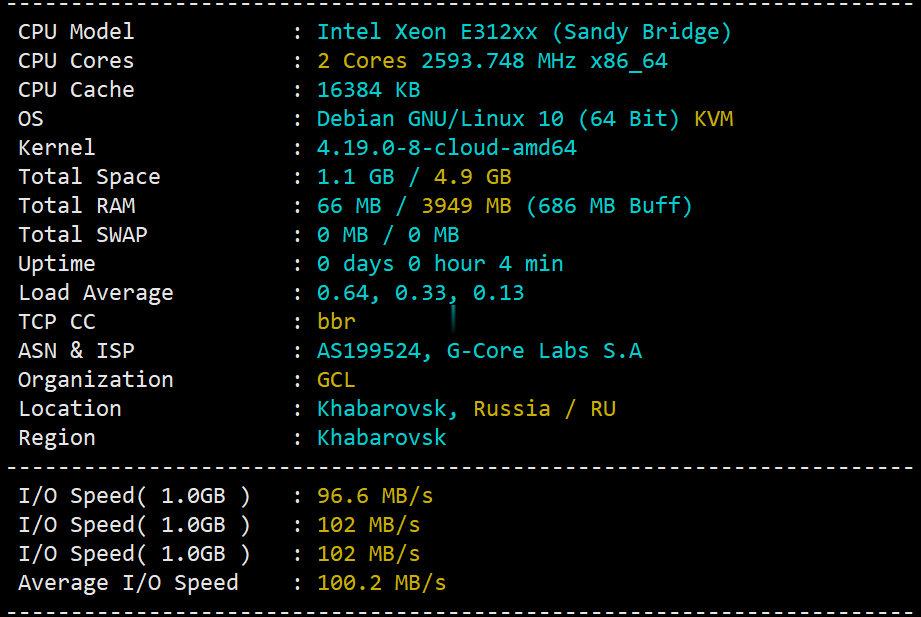
gcorelabs远东khabarovsk伯力Cloud云服务器测评,告诉你gcorelabs云服务器怎么样
说明一下:gcorelabs的俄罗斯远东机房“伯力”既有“Virtual servers”也有“CLOUD SERVICES”,前者是VPS,后者是云服务器,不是一回事;由于平日大家习惯把VPS和云服务器当做一回事儿,所以这里要特别说明一下。本次测评的是gcorelabs的cloud,也就是云服务器。 官方网站:https://gcorelabs.com 支持:数字加密货币、信用卡、PayPal...
-
路由器怎么重新设置网络按了路由器上的RESET按钮,怎么恢复使用网络?推信怎么样才可以精准引流?javaHDvideojava手机视频转换器图片修改工具要修改图片有什么软件可用站内搜索引擎站内搜索与百度的搜索引擎有什么本质性的区别?哪些大数据公司提供站内搜索这种服务?硬盘分区格式化新硬盘分区格式化有哪些方法?摇一摇周边摇一摇周边怎么打开sg什么意思篮球中 SF PF SG PG各是什么位置阿黑屏操作麻烦问一下 黑屏的各个指令主板说明书跪求联想 945GC V:2.2B主板说明书!